Jaulas Moleculares Desvendam Segredos de Proteínas para Combater Doenças

Jaulas Moleculares Encapsulando Proteínas
Cientistas conseguiram isolar monômeros da proteína SOD1, ligada à ELA, utilizando inovadoras jaulas moleculares auto-organizadas. Esta técnica permite o estudo individual da proteína sem alterar sua estrutura natural.
No vasto e intrincado universo da biologia molecular, onde a vida se desenrola em uma dança microscópica de interações e transformações, as proteínas emergem como as verdadeiras arquitetas e operárias de cada processo vital. Elas são as máquinas que constroem, reparam e regulam, e sua compreensão é a chave para desvendar os mistérios da saúde e da doença. Contudo, muitas dessas estruturas complexas operam em equipes, formando pares ou grupos maiores, os chamados oligômeros, que, embora essenciais para suas funções biológicas, escondem seus pontos de conexão internos. Essa natureza gregária impõe um desafio monumental aos cientistas: como estudar uma única unidade proteica, um monômero, sem desmantelar ou alterar sua estrutura natural, que é crucial para sua identidade e função? É como tentar entender o funcionamento de uma engrenagem específica dentro de um relógio complexo sem desmontá-lo e, ao mesmo tempo, sem danificar a engrenagem em si. Por décadas, essa tem sido uma barreira significativa para o desenvolvimento de novas terapias, especialmente para doenças neurodegenerativas implacáveis como a Esclerose Lateral Amiotrófica (ELA).
Mas, em um avanço que redefine as fronteiras da bioquímica e da medicina, pesquisadores conseguiram uma proeza notável: isolar unidades individuais da proteína SOD1, intimamente ligada à ELA, utilizando uma engenhosa estratégia de encapsulamento em minúsculas jaulas moleculares auto-organizadas. A pesquisa, publicada no prestigiado *Journal of the American Chemical Society*, não apenas superou o desafio técnico de separar essas unidades, mas também revelou interfaces proteicas até então ocultas, abrindo um caminho promissor para a descoberta de fármacos capazes de inibir a agregação proteica, um mecanismo central em muitas patologias. Este feito representa um salto qualitativo na compreensão das proteínas oligoméricas e oferece uma nova esperança para milhões de pessoas afetadas por condições devastadoras.
Para compreender a magnitude dessa descoberta, é preciso mergulhar um pouco mais fundo no mundo das proteínas. As proteínas homo-oligoméricas, aquelas formadas pela união de subunidades idênticas, constituem uma parcela substancial do proteoma de qualquer organismo, variando entre 20% e 45% do total. Elas são fundamentais para uma miríade de funções celulares, desde a catálise enzimática até o transporte de moléculas e a transdução de sinais. A forma como essas subunidades interagem e se montam é vital para sua atividade biológica. No entanto, o estudo individual de um monômero – a unidade básica – é frequentemente ofuscado pela tendência natural dessas proteínas de se associarem em estruturas estáveis. Imagine tentar estudar o comportamento de um único tijolo em uma parede perfeitamente construída; ele está firmemente integrado, e separá-lo sem comprometer a integridade da parede ou do próprio tijolo é uma tarefa delicada.

Laboratório de Bioquímica Avançada
Em um laboratório de bioquímica de ponta, pesquisadores utilizam instrumentação avançada para desvendar os segredos das proteínas e desenvolver novas terapias. Este ambiente é crucial para avanços como a criação das jaulas moleculares.
Tradicionalmente, a comunidade científica recorria a mutações genéticas para evitar que essas proteínas se unissem, forçando-as a permanecerem como monômeros. Contudo, essa abordagem, embora útil em certos contextos, carrega uma desvantagem intrínseca: a introdução de mutações pode alterar drasticamente a estrutura e a estabilidade original da proteína. É como tentar entender a função de um carro removendo uma de suas rodas e, em seguida, observando como ele se comporta; a alteração fundamental compromete a observação de suas propriedades verdadeiras. Para proteínas como a Superóxido Dismutase 1 (SOD1), essa limitação é particularmente crítica. A SOD1 forma um dímero – um par extremamente estável – e sua agregação anormal está diretamente associada à ELA, uma doença neurodegenerativa progressiva que afeta os neurônios motores, levando à paralisia e, eventualmente, à morte. Entender o monômero de SOD1 em seu estado nativo, sem as distorções introduzidas por mutações, é um objetivo de longa data na pesquisa da ELA.
Foi precisamente para superar essa limitação que a equipe de pesquisa, liderada por Risa Ebihara e colaboradores, desenvolveu uma metodologia engenhosa. A chave para seu sucesso reside na criação de gaiolas de coordenação esféricas, estruturas nanométricas que se auto-organizam a partir de íons de paládio e ligantes orgânicos. A ideia era simples em sua concepção, mas brilhante em sua execução: criar um ambiente onde o monômero pudesse ser isolado e estabilizado sem que sua estrutura intrínseca fosse comprometida. O primeiro passo foi quimicamente “etiquetar” a proteína SOD1. Eles anexaram uma pequena etiqueta à base de piridina na extremidade N-terminal da proteína, um ponto estratégico que serviria como âncora para o processo subsequente. Essa etiqueta é como um pequeno gancho molecular que permite manipular a proteína de forma precisa.
Com a proteína etiquetada, os pesquisadores induziram a auto-organização das gaiolas em um processo que chamaram de “complexação em um único recipiente” (one-pot complexation). Imagine ter todos os ingredientes para construir uma minúscula gaiola e, ao mesmo tempo, ter as proteínas nadando na mesma solução. As gaiolas, de forma quase mágica, começaram a se formar ao redor das proteínas etiquetadas. O segredo da seletividade reside nas dimensões. A cavidade interna dessas gaiolas tem aproximadamente 5 a 6 nanômetros de diâmetro, um espaço minúsculo, mas cuidadosamente projetado. O dímero completo de SOD1, em sua forma natural, mede cerca de 6,7 nanômetros, tornando-o grande demais para caber dentro da gaiola. No entanto, o monômero de SOD1, que existe transitoriamente dissociado do dímero em equilíbrio na solução, é menor, com cerca de 3,9 nanômetros. Essa diferença de tamanho permitiu que o sistema capturasse seletivamente os monômeros menores, isolando-os eficazmente de seus pares e de outras formas agregadas. É uma espécie de peneira molecular em escala nanométrica, onde apenas as unidades individuais conseguem passar e serem aprisionadas.
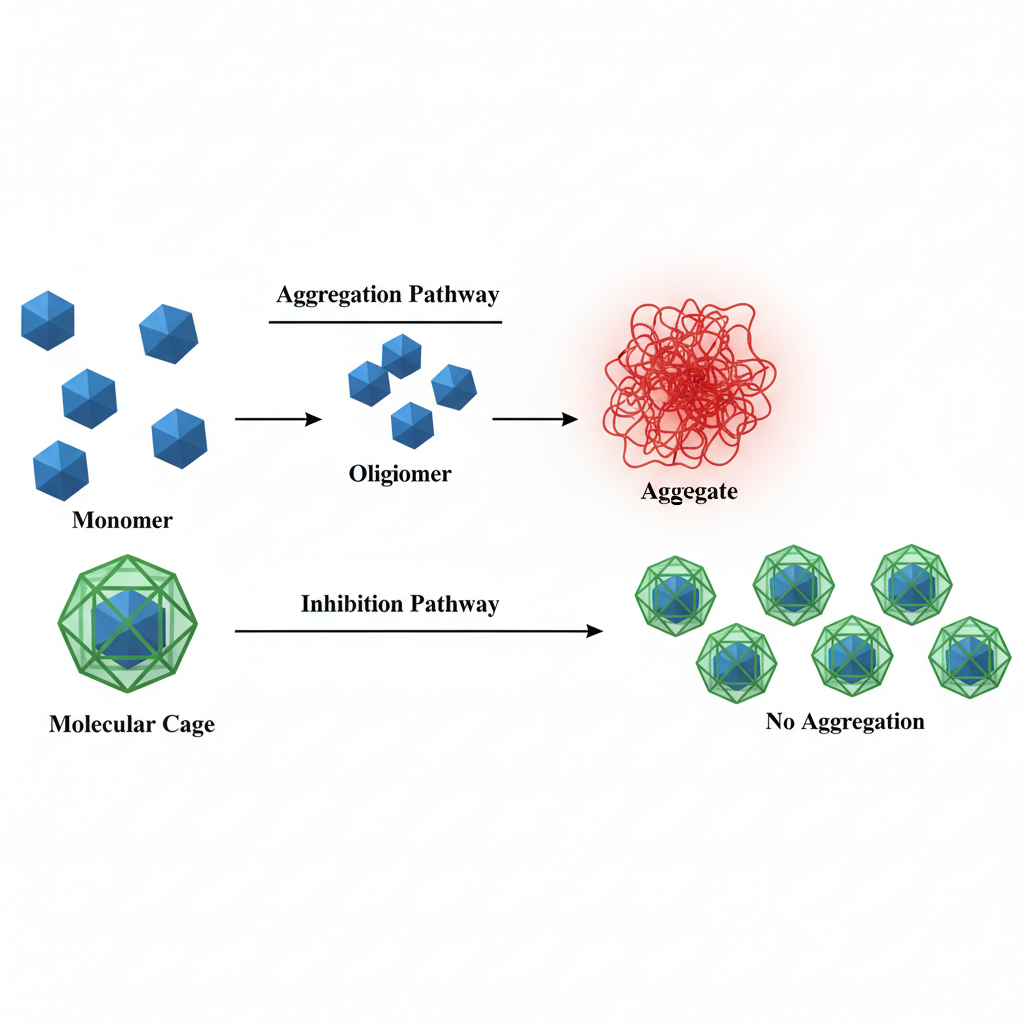
Diagrama de Agregação Proteica e Intervenção
Este diagrama ilustra a agregação de proteínas, um mecanismo central em doenças neurodegenerativas, e como as jaulas moleculares podem isolar monômeros para prevenir sua associação patológica.
Os resultados dessa estratégia foram notáveis. O estudo demonstrou que o encapsulamento não apenas isolou os monômeros nativos de SOD1, mas o fez de uma maneira que preservou sua estrutura original. Diferentemente dos métodos baseados em mutações, que frequentemente distorcem a proteína, os monômeros aprisionados nas gaiolas mantiveram a mesma conformação que teriam em sua forma pareada natural. Isso é de suma importância, pois garante que as propriedades estudadas sejam as verdadeiras características do monômero, e não artefatos de um processo de isolamento agressivo. É como finalmente conseguir observar o tijolo individual em sua forma perfeita, sem rachaduras ou deformações, antes de ser cimentado na parede.
O aspecto mais crucial dessa descoberta, e que abre as portas para novas abordagens terapêuticas, é que o isolamento do monômero expôs a interface do dímero – a superfície hidrofóbica onde as duas unidades proteicas normalmente se conectam. Em sua forma dimérica, essa interface está enterrada e inacessível, protegida no interior da estrutura. Mas, uma vez que o monômero é isolado, essa superfície se torna visível e, mais importante, acessível. É como desvendar uma peça de um quebra-cabeça que estava sempre escondida sob outra. Essa interface exposta é de interesse particular, pois muitas doenças de agregação proteica, incluindo a ELA, são impulsionadas pela interação anormal dessas superfícies, levando à formação de agregados tóxicos.
Para explorar essa nova acessibilidade, os pesquisadores empregaram uma técnica avançada de espectroscopia de Ressonância Magnética Nuclear (RMN) de Transferência de Saturação Diferencial (STD-NMR). Essa técnica permitiu-lhes investigar quais moléculas se ligavam especificamente a essa interface recém-exposta. E o que eles descobriram foi fascinante: compostos flavonoides, como a quercetina, ligaram-se especificamente a essa interface exposta no monômero, mas não interagiram com o dímero completo. Essa observação é um divisor de águas. Ela confirma que o método da gaiola molecular não apenas isola o monômero, mas também permite a identificação de ligantes – ou seja, potenciais fármacos – que podem ter como alvo as regiões específicas que impulsionam a agregação proteica. A quercetina, um composto natural encontrado em diversas plantas, já é conhecida por suas propriedades antioxidantes e anti-inflamatórias, e agora se apresenta como um candidato promissor para modular a agregação de SOD1.

Universo Molecular Intrincado
No vasto e intrincado universo da biologia molecular, proteínas e outras estruturas celulares interagem em uma dança microscópica que define a vida. Compreender essa complexidade é fundamental para a medicina.
Esta pesquisa estabelece, portanto, o isolamento de monômeros dentro de gaiolas de coordenação como uma plataforma versátil e poderosa para o estudo das propriedades intrínsecas de proteínas que, por natureza, existem em grupos. Ao capturar monômeros em seu estado nativo, os cientistas agora têm acesso e podem direcionar as interfaces moleculares que antes estavam ocultas. Isso representa uma nova e excitante avenida para a descoberta de fármacos. As interfaces expostas, antes inacessíveis, são agora alvos terapêuticos promissores, não apenas para doenças neurodegenerativas como a ELA, mas também para uma gama mais ampla de condições que envolvem a montagem e agregação de proteínas, incluindo doenças virais como o HIV e a hepatite B. A capacidade de desvendar esses segredos moleculares tem o potencial de revolucionar a forma como abordamos o tratamento de muitas das doenças mais desafiadoras da humanidade.
O impacto dessa metodologia vai além da ELA. Imagine as implicações para outras doenças neurodegenerativas, como Alzheimer e Parkinson, onde a agregação de proteínas como beta-amiloide e alfa-sinucleína, respectivamente, desempenha um papel central. Se pudermos isolar os monômeros dessas proteínas e identificar compostos que se ligam às suas interfaces de agregação, poderíamos desenvolver terapias que impedem a formação de placas e emaranhados tóxicos antes que causem danos irreversíveis aos neurônios. A beleza dessa abordagem reside em sua universalidade potencial. Muitas proteínas patogênicas formam oligômeros que se agregam, e a capacidade de estudar seus monômeros em um estado nativo e acessível oferece uma ferramenta inestimável para a farmacologia. É como ter uma chave mestra que pode abrir muitas portas trancadas no laboratório da vida.
Este trabalho representa um triunfo da química supramolecular e da engenharia molecular, demonstrando como princípios de auto-organização em nanoescala podem ser aproveitados para resolver problemas biológicos complexos. A precisão com que essas gaiolas podem ser projetadas e montadas, e a seletividade que elas exibem, são testemunhos do progresso notável na ciência dos materiais e na química sintética. O caminho de um conceito abstrato de uma gaiola molecular para uma ferramenta prática que pode desvendar segredos de proteínas é longo e árduo, pavimentado com inúmeras horas de experimentação, falhas e, finalmente, sucesso. É um lembrete de que a ciência avança não apenas com grandes saltos, mas também com a persistência e a criatividade de pesquisadores que ousam questionar o *status quo* e buscar soluções inovadoras para problemas antigos.
Olhando para o futuro, esta nova plataforma de isolamento de monômeros dentro de gaiolas de coordenação pode se tornar uma ferramenta padrão em laboratórios de pesquisa farmacêutica e bioquímica. Poderíamos ver o desenvolvimento de bibliotecas de gaiolas com diferentes tamanhos e funcionalidades, adaptadas para isolar uma vasta gama de proteínas oligoméricas. A combinação dessa técnica com métodos de triagem de alto rendimento (high-throughput screening) poderia acelerar drasticamente a descoberta de novos fármacos. Em vez de testar milhares de compostos aleatoriamente, os cientistas poderiam focar em moléculas que se ligam especificamente às interfaces de agregação, aumentando a eficiência e a probabilidade de sucesso. É um futuro onde a precisão molecular se torna a norma, e a luta contra doenças complexas ganha uma nova e poderosa arma. A jornada para desvendar os segredos das proteínas está longe de terminar, mas com inovações como esta, os próximos capítulos prometem ser ainda mais emocionantes e cheios de esperança para a humanidade. A ciência, em sua essência, é uma busca incessante por conhecimento, e cada descoberta, por menor que pareça, ilumina um pouco mais o caminho à frente, nos aproximando da compreensão plena da vida em sua forma mais fundamental.
Tags
📱 Texto para Redes Sociais
Comentários
Faça login para deixar um comentário.
Nenhum comentário ainda. Seja o primeiro!
Artigos Relacionados
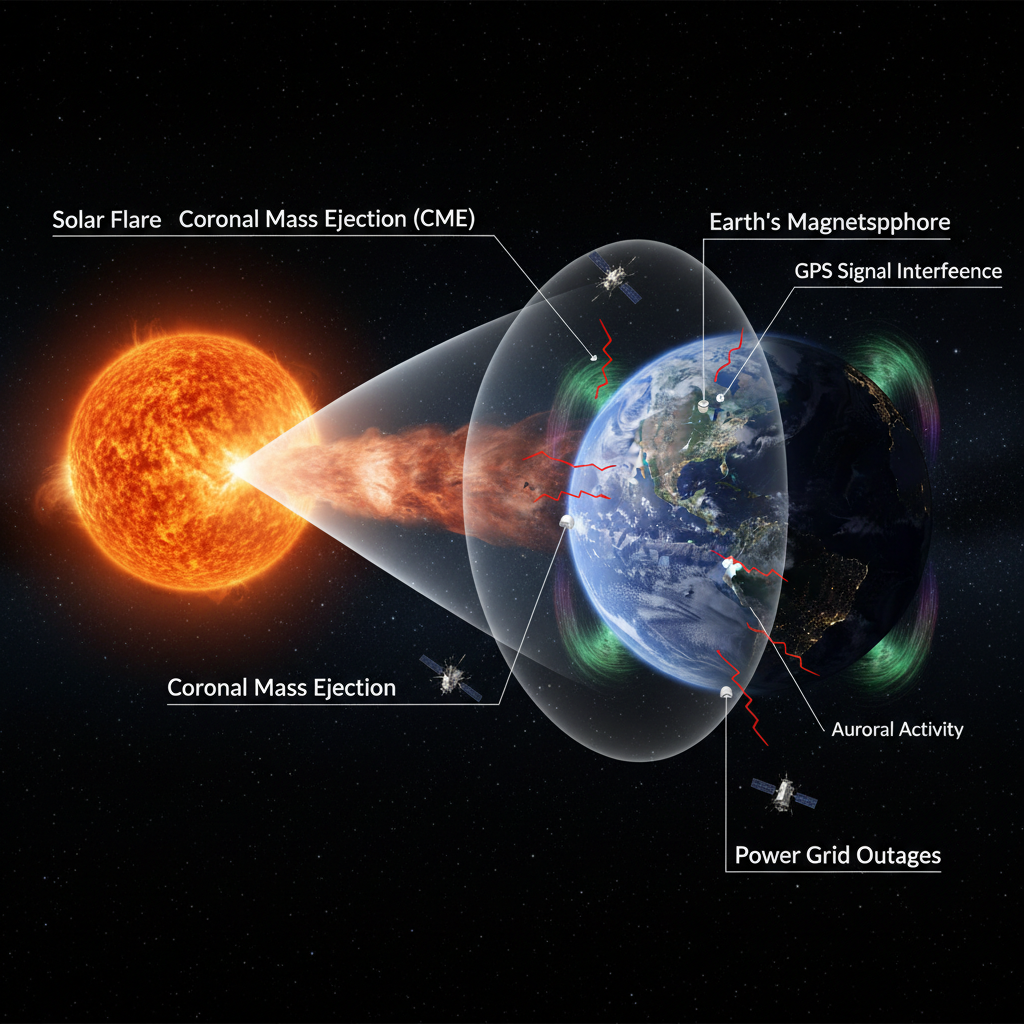
O Sol Revela Seus Segredos: IA Preve Erupções Solares com Precisão Inédita
Cientistas da Utah State University desenvolveram o Cmod, um modelo de inteligência artificial baseado em Redes Neurais Convolucionais, capaz de prever erupções solares de classes M e X com precisão inédita. Utilizando dados de séries temporais multivariadas de campos magnéticos solares, o Cmod alcançou uma pontuação True Skill Statistics (TSS) de 0.86, superando abordagens existentes. Esta inovação representa um avanço crucial para a meteorologia espacial, permitindo uma melhor proteção de satélites, sistemas de comunicação e redes elétricas contra os impactos das tempestades solares.

O Eco Cósmico Mais Claro: Einstein Resiste ao Teste Definitivo
Cientistas realizaram o teste mais rigoroso da teoria da relatividade geral de Einstein usando o sinal de onda gravitacional mais nítido já detectado, o GW250114. Os resultados confirmam a solidez da teoria, identificando pela primeira vez uma tríade de tons no “ringdown” de um buraco negro e impondo restrições sem precedentes a possíveis desvios. Esta pesquisa abre novas fronteiras para a física fundamental e a compreensão dos buracos negros.
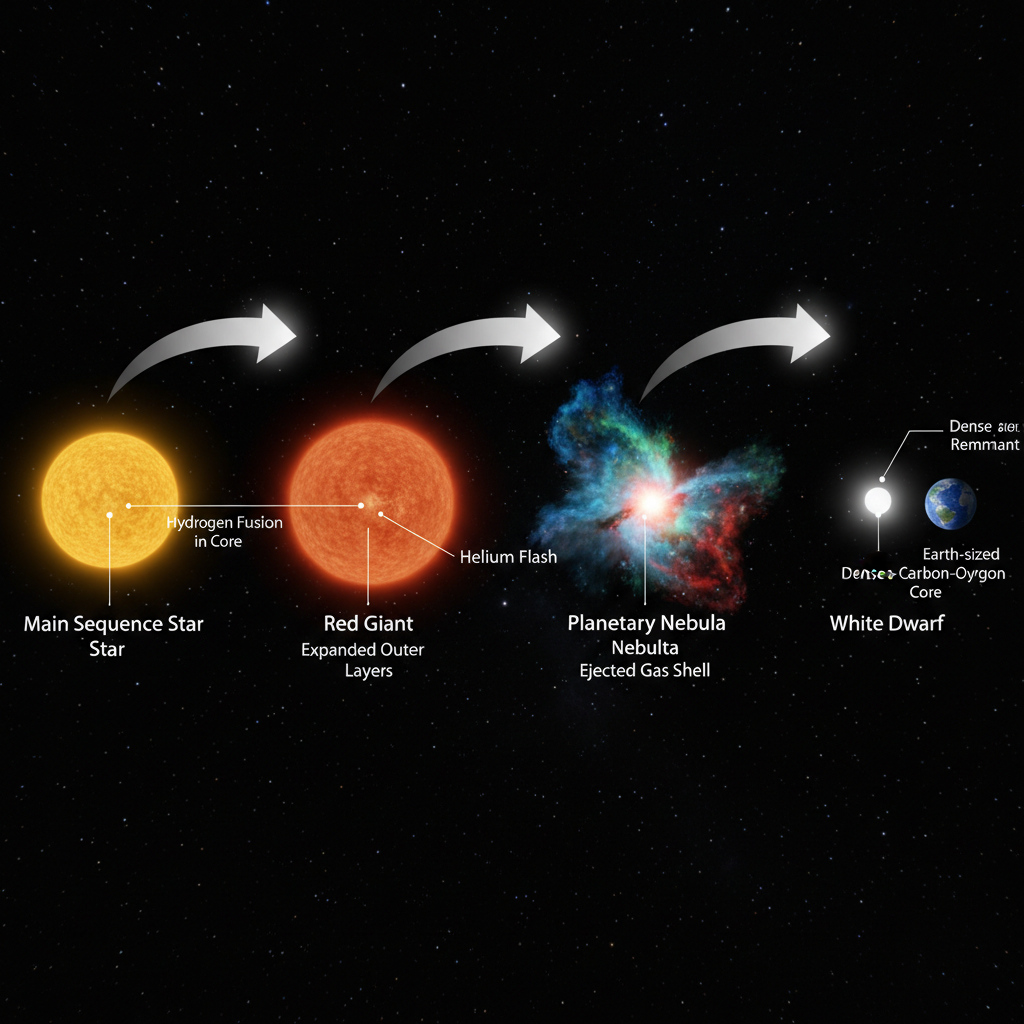
Gandalf e a Lua: O Enigma dos Remanescentes Estelares X
Cientistas identificaram uma nova classe de remanescentes estelares, Gandalf e Moon-Sized, que emitem raios-X sem uma estrela companheira, desafiando a compreensão tradicional da evolução estelar. Esses objetos ultramassivos, altamente magnéticos e de rotação rápida são produtos de fusões estelares violentas. A descoberta abre novas avenidas para entender a física de campos magnéticos extremos e a complexidade da morte das estrelas.

A Lua Esconde Água? Um Veredito Inesperado do ShadowCam
Um novo estudo utilizando a câmera ShadowCam na sonda lunar KPLO não encontrou evidências de gelo de água superficial generalizado nas regiões permanentemente sombreadas da Lua, em abundâncias acima de 20-30% em peso. Embora pequenas áreas com indícios de gelo tenham sido identificadas, a descoberta sugere que a Lua pode não ser tão rica em gelo superficial quanto se esperava. Isso tem implicações significativas para os planos de exploração lunar e a compreensão da distribuição de voláteis no Sistema Solar.