A Dança Cósmica das Células: Miosina Quiral e os Anéis Giratórios da Vida

Miosina Quiral e Anéis Celulares
Uma representação artística e cientificamente informada da miosina quiral organizando filamentos de actina em anéis rotatórios dentro de uma célula, ilustrando a auto-organização molecular que impulsiona processos biológicos fundamentais.
No intrincado balé da vida, onde cada célula pulsa com uma orquestra molecular de tirar o fôlego, a ordem emerge de um caos aparente. Não há um maestro central ditando cada movimento, nem um projeto arquitetônico rígido que defina a estrutura de um organismo. Em vez disso, a complexidade e a organização que observamos, desde a formação de um embrião até o movimento coordenado de nossos músculos, brotam de interações incessantes entre bilhões de moléculas que se movem e se rearranjam a cada instante. É um espetáculo de auto-organização, um testemunho da capacidade intrínseca da matéria viva de construir estruturas funcionais sem a necessidade de um plano predefinido. Entre os exemplos mais notáveis dessa ordem emergente está a assimetria esquerda-direita, uma propriedade fundamental que permeia a biologia em todas as suas escalas, desde a orientação de moléculas individuais até a disposição de órgãos em um corpo. Essa quiralidade, a característica que torna um objeto distinto de sua imagem espelhada, é vital para inúmeros processos biológicos e pode ser observada em toda a natureza, desde a espiral de um caracol até a forma de nossas próprias mãos. A questão de como essa ordem, tanto em pequena quanto em grande escala, surge das interações de componentes microscópicos tem sido uma das indagações mais profundas da biologia, um enigma que desafia a compreensão e impulsiona a pesquisa.
É como tentar entender a formação de uma galáxia espiral a partir da gravidade de incontáveis estrelas e gás, mas no microcosmo celular. Para desvendar essa lacuna de conhecimento, cientistas têm dedicado esforços consideráveis ao estudo das biomoléculas que impulsionam o movimento dentro das células. Duas dessas estrelas moleculares, o actina e a miosina, são exemplos perfeitos de como a natureza concebeu mecanismos elegantes para realizar tarefas complexas. A actina, uma proteína abundante, forma uma rede dinâmica de filamentos que confere às células sua forma, sustentando sua arquitetura e facilitando o transporte de materiais internos. Pense nela como o andaime e as estradas de uma cidade celular em constante reconstrução. A miosina, por sua vez, é uma família de minúsculos “motores moleculares”, verdadeiras máquinas nanométricas que convertem energia química, obtida da quebra de ATP, em força mecânica. São os trabalhadores incansáveis que puxam, empurram e transportam cargas pela rede de actina.

Laboratório de Biologia Molecular
O ambiente de um laboratório de biologia molecular, onde cientistas desvendam os segredos das interações celulares, utilizando tecnologia de ponta para observar e manipular as moléculas da vida.
Juntas, actina e miosina são a dupla dinâmica por trás de processos biológicos cruciais, como a contração muscular em animais, permitindo-nos mover, respirar e viver, e o fluxo citoplasmático em células vegetais, um movimento essencial para a distribuição de nutrientes e organelas. No entanto, apesar de sua importância onipresente, a maneira exata pela qual as interações aparentemente simples entre essas duas proteínas podem gerar estruturas assimétricas em uma escala que abrange a célula inteira, especialmente na ausência de qualquer modelo guia ou influência externa, permaneceu um mistério intrigante. É como observar um grupo de formigas construindo uma colônia complexa sem um arquiteto ou um projeto pré-definido, apenas seguindo regras simples de interação. Motivados por essa questão fundamental, uma equipe de pesquisa visionária, liderada pelo Professor Kohji Ito e pelo Dr. Takeshi Haraguchi, ambos da Graduate School of Science da Chiba University, no Japão, embarcou em uma jornada para investigar como a ordem pode emergir apenas das interações entre actina e miosina. O estudo deles, publicado na prestigiada revista *Proceedings of the National Academy of Sciences*, concentrou-se em uma proteína motora vegetal de ação rápida, conhecida como miosina XI de *Chara corallina* (CcXI). A escolha dessa miosina específica não foi aleatória; ela é conhecida por sua eficiência e por desempenhar um papel crucial no transporte intracelular em algas, um modelo biológico fascinante para o estudo de processos celulares fundamentais.
A colaboração se estendeu a outros pesquisadores notáveis, como o Dr. Yasuhiro Inoue da Kyoto University, o Dr. Toshifumi Mori da Kyushu University e o Dr. Kenji Matsuno da The University of Osaka, unindo expertises diversas para abordar o problema de forma abrangente. Essa união de mentes e recursos é um reflexo da natureza colaborativa da ciência moderna, onde as grandes descobertas frequentemente nascem da sinergia entre diferentes laboratórios e perspectivas. Em seus experimentos meticulosos, os pesquisadores empregaram um sistema de laboratório simplificado, uma abordagem elegante que permite isolar e estudar componentes específicos em um ambiente controlado, longe da complexidade esmagadora de uma célula viva. Eles combinaram filamentos de actina purificados e miosina XI com ATP, a molécula universal de energia que alimenta a atividade motora.
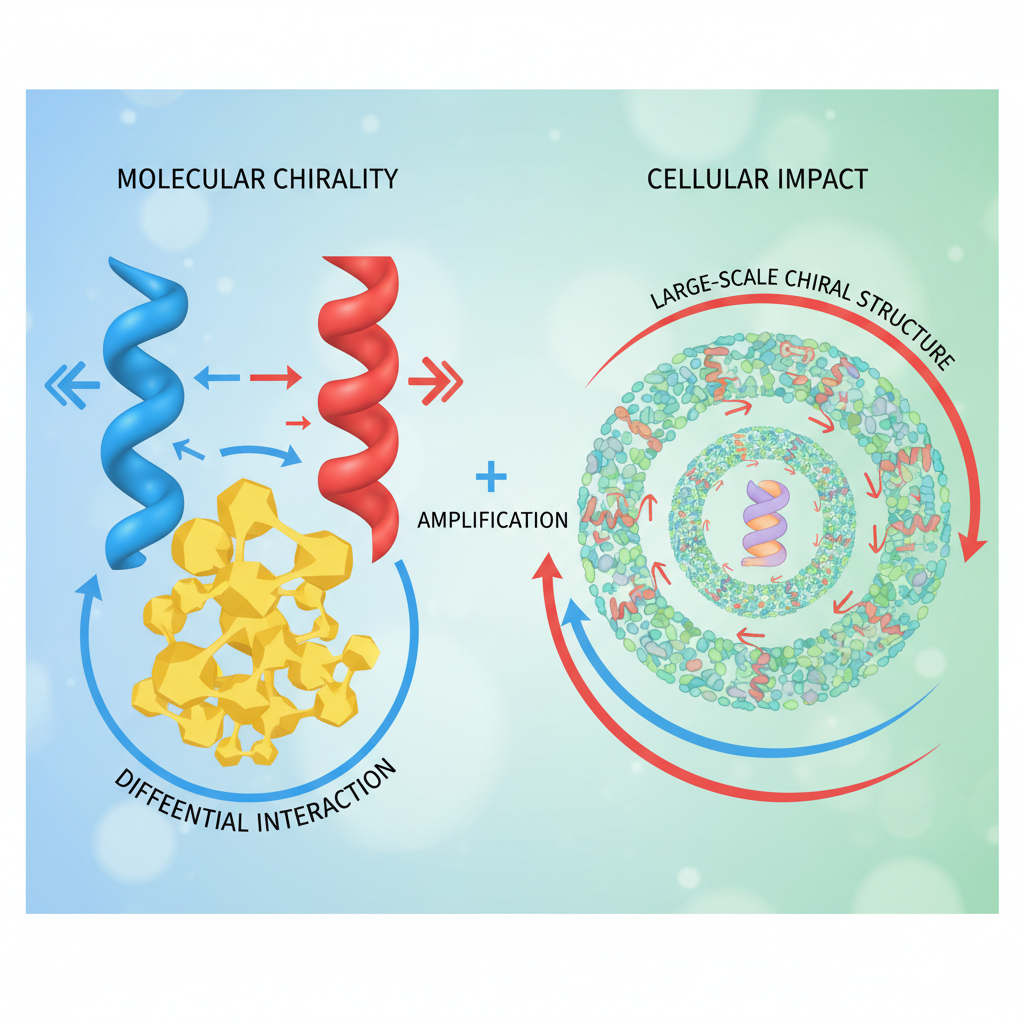
Diagrama de Quiralidade Molecular
Diagrama esquemático que ilustra o conceito de quiralidade molecular, mostrando como a assimetria em nível molecular pode gerar estruturas organizadas e direcionais em escala celular, como os anéis de actina.
Sob essas condições aparentemente simples, os cientistas testemunharam um comportamento inesperado e profundamente revelador. Em vez de formar padrões aleatórios ou fluir coletivamente em uma única direção, os filamentos de actina se auto-organizaram espontaneamente em estruturas estáveis, em forma de anel, com um tamanho aproximadamente comparável ao de uma célula. O que era ainda mais notável é que esses anéis giravam continuamente em uma única direção, mantendo-se fixos no lugar, mesmo enquanto filamentos individuais continuavam a se mover e se rearranjar dentro deles. Era como observar um pequeno redemoinho molecular, uma dança coreografada onde cada partícula contribuía para um movimento coletivo e persistente. Essa observação foi um momento de eureka, pois demonstrava a capacidade intrínseca dessas moléculas de gerar ordem e movimento complexos a partir de interações básicas, sem qualquer intervenção externa ou modelo preexistente. A beleza dessa descoberta reside na sua simplicidade e na sua profundidade, revelando um princípio fundamental da auto-organização biológica. Uma investigação mais aprofundada revelou que esse comportamento coletivo extraordinário tem sua origem na maneira particular como os filamentos de actina individuais são impulsionados pela CcXI.
Ao contrário de muitas outras miosinas, que tendem a mover os filamentos em trajetórias retas, a CcXI os impulsiona ao longo de caminhos curvos. Essa curvatura, um detalhe sutil mas crucial, surge na ponta principal de cada filamento, onde passos repetidos impulsionados pelo motor gradualmente inclinam sua direção de movimento. É como se cada motor individual tivesse uma pequena preferência de virar, e a soma dessas pequenas preferências resultasse em um caminho curvo para o filamento como um todo. Quando muitos desses filamentos curvos interagem em uma densidade suficientemente alta, eles naturalmente se alinham e se fecham em anéis giratórios, criando uma estrutura quiral estável sem qualquer orientação externa. É um exemplo primoroso de como as propriedades em microescala podem levar a fenômenos emergentes em macroescala. Para validar ainda mais essa interpretação e explorar os parâmetros que governam esse comportamento, os pesquisadores realizaram simulações computacionais sofisticadas. Essas simulações, que replicam as interações moleculares em um ambiente virtual, demonstraram que a curvatura do filamento é um requisito chave para a formação dos anéis.

Galáxia Espiral e Célula Cósmica
Uma imagem impactante que justapõe a majestade de uma galáxia espiral com a complexidade de uma célula, visualizando a analogia entre a formação de estruturas cósmicas e a auto-organização molecular da vida.
Além disso, as simulações revelaram que o tamanho dos anéis reproduzidos era determinado pelo grau de curvatura dos filamentos, estabelecendo uma relação direta entre uma propriedade molecular intrínseca e a escala da estrutura emergente. Essa combinação de experimentos empíricos e modelagem computacional é uma marca registrada da pesquisa de ponta, permitindo que os cientistas testem hipóteses e obtenham *insights* que seriam impossíveis de alcançar apenas com um método. O Professor Ito, um dos líderes da pesquisa, comentou com entusiasmo sobre as implicações de suas descobertas, afirmando que “as estruturas em forma de anel formadas em nossos experimentos se assemelham muito ao alinhamento uniformemente polarizado de filamentos de actina observado em células vegetais.” Essa observação é crucial, pois sugere que o processo de auto-organização identificado no laboratório não é apenas uma curiosidade de um sistema simplificado, mas representa um princípio fundamental que opera dentro das células vivas. “Isso sugere que o processo de auto-organização identificado aqui representa um princípio fundamental que se mantém mesmo em sistemas reconstituídos simplificados e captura o mecanismo essencial subjacente ao alinhamento da actina em células vivas”, explicou ele. Essas palavras ressoam com a profundidade de uma descoberta que transcende o experimento em si, apontando para uma compreensão mais universal dos mecanismos da vida. Em conjunto, esses achados ajudam a esclarecer como as células vegetais podem organizar sua arquitetura interna para promover o transporte molecular eficiente através de redes de actina auto-organizadas. É um passo significativo para desvendar os segredos da logística celular, um sistema de transporte que supera em complexidade e eficiência qualquer rede que a humanidade já construiu.
A capacidade de compreender e, eventualmente, controlar esses processos tem implicações de longo alcance. O Professor Ito também vislumbrou o impacto futuro de seu trabalho, destacando que “ao aprofundar nossa compreensão dos princípios que governam o crescimento celular e o transporte intracelular em células vegetais, nossos resultados podem contribuir com conhecimento fundamental para controlar o crescimento das plantas e melhorar a produtividade agrícola.” Imagine um futuro onde, ao entender os motores moleculares que impulsionam o crescimento das plantas, possamos otimizar a produção de alimentos, tornando as culturas mais resistentes e produtivas. Essa é a promessa da ciência básica: descobertas que, à primeira vista, podem parecer distantes de aplicações práticas, mas que pavimentam o caminho para inovações transformadoras. Além da biologia vegetal, os resultados desta pesquisa têm implicações mais amplas para a ciência dos materiais e a bioengenharia. A capacidade de sistemas de gerar ordem e movimento de forma autônoma a partir de componentes simples poderia inspirar novas abordagens para o design de biomateriais ativos ou nanomaquinaria. Pense em materiais que podem se auto-reparar, ou robôs em escala nanométrica que podem realizar tarefas complexas dentro do corpo humano, tudo isso inspirado nos princípios de auto-organização que governam a vida. A natureza, com sua engenhosidade de bilhões de anos, oferece um vasto catálogo de soluções para os desafios da engenharia e da medicina.
Este trabalho, portanto, não é apenas uma janela para a biologia celular, mas também um farol para a inovação em diversas áreas da ciência e da tecnologia. Em sua essência, este trabalho ressalta a emergência da auto-organização não como um resultado misterioso ou excessivamente complexo, mas como um processo previsível, governado por princípios físicos simples que podemos, e estamos, começando a compreender. É um lembrete de que a vida, em toda a sua magnificência, é construída sobre uma base de interações moleculares que, embora individualmente simples, dão origem a uma complexidade estonteante. A ciência, ao desvendar esses princípios, não diminui o encanto da vida, mas o amplifica, revelando a elegância e a inteligência inerentes ao universo. A jornada para decifrar os segredos da auto-organização celular continua, e cada descoberta nos aproxima de uma compreensão mais profunda de como a vida funciona, de como a ordem emerge do que parece ser um caos molecular. E, como sempre, a cada resposta encontrada, novas perguntas surgem, impulsionando a curiosidade humana a explorar ainda mais os confins do conhecimento, tanto no vasto cosmos quanto no íntimo universo de uma única célula. É a eterna busca por entender nosso lugar no universo, e a vida que o habita, em todas as suas formas e escalas, um testemunho da incansável paixão humana por desvendar os mistérios que nos cercam, desde a dança das galáxias até o giro silencioso dos anéis de actina dentro de uma célula vegetal.
Tags
📱 Texto para Redes Sociais
Comentários
Faça login para deixar um comentário.
Nenhum comentário ainda. Seja o primeiro!